Tentang Fornas
Sesuai dengan UU No. 17 Tahun 2023 tentang Kesehatan menyatakan bahwa Pemerintah menyusun daftar dan jenis obat yang secara esensial harus tersedia bagi kepentingan masyarakat, dan didalam UU No.40 tahun 2004 tentang Sistem Jaminan Kesehatan Nasional (SJSN) yang dielaborasi dalam Peraturan Presiden No. 82 tahun 2018 tentang Jaminan Kesehatan menyatakan bahwa Pelayanan Obat, Alat Kesehatan dan BMHP untuk peserta jaminan kesehatan pada Fasilitas Kesehatan berpedoman pada daftar obat, alat kesehatan dan BMHP yang ditetapkan oleh Menteri.
Formularium Nasional (Fornas) adalah daftar obat terpilih yang dibutuhkan dan digunakan sebagai acuan penulisan resep pada pelaksanaan pelayanan kesehatan dalam penyelenggaraan program jaminan kesehatan. Fornas digunakan sebagai pedoman pelayanan obat untuk peserta jaminan kesehatan pada fasilitas pelayanan kesehatan. Fornas memuat daftar obat esensial nasional yang merupakan daftar obat esensial terpilih yang paling dibutuhkan dan harus tersedia di Fasilitas Pelayanan Kesehatan Tingkat Pertama (FPKTP) dan Fasilitas Pelayanan Kesehatan Tingkat Lanjut (FPKTL) sesuai dengan kebutuhan pelayanan kesehatan. Daftar esensial nasional tersebut harus diterapkan secara konsisten dan terus-menerus dalam pemberian pelayanan kesehatan di fasilitas pelayanan kesehatan
Peninjauan Fornas dilakukan paling lama 2 (dua) tahun sekali, namun apabila diperlukan dapat dilakukan perubahan (adendum) sebelum 2 (dua) tahun untuk menyesuaikan dengan kemajuan ilmu pengetahuan, memberikan ruang perbaikan terhadap isi Fornas, serta meningkatkan kecepatan akses dalam penggunaan dan penyerahan obat kepada pasien yang disesuaikan dengan kompetensi tenaga kesehatan dan tingkat fasilitas pelayanan kesehatan yang ada.
Penyusunan Fornas dimulai pertama kali pada tahun 2013. Hingga saat ini, Fornas telah mengalami 5 kali revisi dan 7 kali perubahan (adendum). Pada tahun 2023 (revisi ke-5) telah ditetapkan KMK No.HK.01.07/MENKES/2197/2023 tentang Formularium Nasional yang berlaku per tanggal 1 Maret 2024, dengan jumlah item obat dalam Fornas berjumlah 672 item zat khasiat dalam 1.132 sediaan/kekuatan yang terbagi dalam 33 kelas terapi.
Fornas tidak hanya berperan pada proses pemilihan dan seleksi obat yang digunakan dalam JKN, namun juga menjadi acuan dalam hal pengadaan melalui E-Purchasing/E-Catalogue. Di dalam Fornas obat-obatan yang bermutu dan cost-effective telah dipilih, dan penggunaannya telah diatur untuk menghindari penggunaan obat yang tidak rasional.
Dengan demikian diharapkan dengan mengimplementasikan penggunaan obat sesuai Fornas dalam pelayanan kesehatan di fasilitas pelayanan kesehatan, maka akan tercapai pelayanan kesehatan yang optimal melalui penggunaan obat rasional dan pasien akan mendapatkan obat terpilih yang tepat, berkhasiat, bermutu, aman, terjangkau dan cost-effective.
Tim Penyusun Fornas
Fornas disusun oleh Komnas Fornas yang merupakan Tim Seleksi Obat yang bertanggung jawab untuk penyusunan Formularium Nasional yang ditetapkan melalui Keputusan Menteri Kesehatan No. HK.01.07/MENKES/1295/2022 tentang Komite Nasional Seleksi Obat dan Fitofarmaka dengan didampingi kelompok kerja yang ditetapkan melalui Keputusan Direktorat Jenderal Kefarmasian dan Alat Kesehatan tentang No. HK.02.02/E/21560/2022 Tim Seleksi Obat Formularium Nasional
Sistematika penulisan Fornas
Dalam penulisan obat pada Fornas terdapat beberapa ketentuan terkait dengan penggolongan obat, penulisan nama obat, ketetapan restriksi, peresepan maksimal, serta pengaturan fasilitas pelayanan kesehatan penyedia obat. Adapun ketentuan penulisan Formularium Nasional adalah sebagai berikut:
| 1. | Sistematika penggolongan nama obat didasarkan pada kelas terapi, subkelas terapi, sub-subkelas terapi, nama generik obat, sediaan/kekuatan, restriksi, tingkat fasilitas pelayanan kesehatan dan peresepan maksimal. |
| 2. | Penulisan nama obat disusun berdasarkan abjad nama obat dan dituliskan sesuai Farmakope Indonesia edisi terkini. Jika tidak ada dalam Farmakope Indonesia, maka digunakan International Non-proprietary Names (INN)/nama generik yang diterbitkan WHO. Obat yang sudah lazim digunakan dan tidak mempunyai nama INN (generik) ditulis dengan nama lazimnya. Obat kombinasi yang tidak mempunyai nama INN (generik) diberi nama yang disepakati sebagai nama generik untuk kombinasi dan dituliskan masing-masing komponen zat berkhasiatnya disertai kekuatan masing-masing komponen. Untuk beberapa hal yang dianggap perlu nama sinonim, dituliskan di antara tanda kurung. |
| 3. | Satu jenis obat dapat tercantum dalam beberapa kelas terapi, subkelas atau sub-subkelas terapi sesuai indikasi medis. Satu jenis obat dapat terdiri dari beberapa bentuk sediaan dan satu bentuk sediaan dapat terdiri dari beberapa jenis kekuatan. |
| 4. | Tanda simbol [P] menunjukkan bahwa obat tersebut pengadaannya disediakan oleh Program Kementerian Kesehatan atau Program BKKBN dengan ketentuan sebagai berikut:
1. Apabila tercantum di belakang nama zat aktif, maka ketentuan ini berlaku untuk semua kekuatan dan bentuk sediaan zat aktif tersebut
2. Apabila tercantum di belakang masing-masing kekuatan atau bentuk sediaan zat aktif tertentu, maka ketentuan ini berlaku hanya untuk kekuatan
atau bentuk sediaan zat aktif tersebut. |
| 5. | Tanda simbol [Ca] yang tercantum di belakang nama zat aktif menunjukkan bahwa obat antineoplastik dan imunomodulator digunakan untuk terapi kanker. |
| 6. | Tanda centang (√) pada kolom FPKTP menunjukkan obat yang dipakai di FPKTP untuk pelayanan kesehatan primer. |
| 7. | Tanda centang (√) dan tulisan “PP” pada kolom FPKTP menunjukkan obat yang dipakai di Puskesmas Perawatan. |
| 8. | Tanda centang (√) pada kolom FPKTL menunjukkan obat yang dipakai di FPKTL untuk pelayanan kesehatan spesialistik atau sub spesialistik. |
| 9. | Tanda bintang (*) menunjukkan bahwa obat tersebut dapat disediakan dan diberikan oleh FPKTP atau Apotek yang bekerjasama dengan BPJS Kesehatan untuk program rujuk balik dengan ketentuan sebagai berikut:
a. Apabila tercantum di belakang nama zat aktif, maka ketentuan ini berlaku untuk semua kekuatan dan bentuk sediaan zat aktif tersebut.
b. Apabila tercantum di belakang masing-masing kekuatan atau bentuk sediaan zat aktif tertentu, maka ketentuan ini berlaku hanya untuk kekuatan
atau bentuk sediaan zat aktif tersebut. |
| 10. | Tanda centang bintang (√*) menunjukkan bahwa initial treatment dilakukan di FPKTL, yang kemudian selanjutnya obat tersebut dapat disediakan dan diberikan oleh FPKTP atau apotek yang bekerjasama dengan BPJS Kesehatan untuk program rujuk balik. |
| 11. | Penulisan restriksi dilakukan dengan ketentuan sebagai berikut:
a. Apabila tercantum di bawah kelas terapi/sub kelas terapi, maka ketentuan ini berlaku untuk semua item obat yang termasuk di dalam kelas
terapi/sub kelas terapi tersebut
b. Apabila tercantum di bawah nama zat aktif, maka ketentuan ini berlaku untuk semua kekuatan dan bentuk sediaan zat aktif tersebut.
c. Apabila tercantum di bawah masing-masing kekuatan atau bentuk sediaan zat aktif tertentu, maka ketentuan ini berlaku hanya untuk kekuatan
atau bentuk sediaan zat aktif tersebut. |
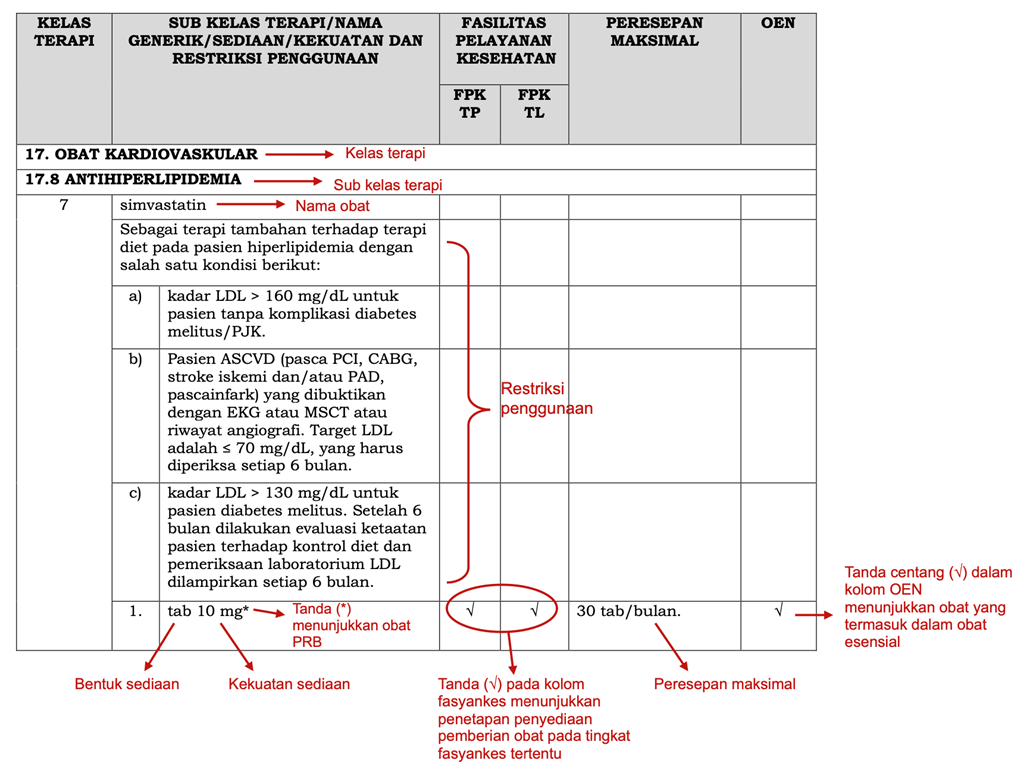
Contoh penulisan obat dalam Fornas:
 |
 |
 |
 |
 |